
 La mayor parte de los compuestos conocidos son orgánicos, ya sea que provengan directamente de los seres vivos o que se produzcan artificialmente. Los compuestos orgánicos se encuentran en gran cantidad de artículos, como alimentos, medicinas, pinturas, detergentes, cosméticos, textiles, combustibles, lubricantes, entre otros.
La mayor parte de los compuestos conocidos son orgánicos, ya sea que provengan directamente de los seres vivos o que se produzcan artificialmente. Los compuestos orgánicos se encuentran en gran cantidad de artículos, como alimentos, medicinas, pinturas, detergentes, cosméticos, textiles, combustibles, lubricantes, entre otros.
Muchas áreas profesionales relacionadas con las ciencias necesitan conocimientos específicos de química; por ejemplo, el petróleo es una mezcla de compuestos orgánicos llamados hidrocarburos, así que todos los campos e industrias donde se usa esta sustancia recurren a conceptos y procedimientos químicos. En este sentido, el petróleo origina una infinidad de materias primas, como plásticos, medicinas, solventes, colorantes, conservadores, fertilizantes, pesticidas, combustibles y muchos otros.

Los compuestos más abundantes en la naturaleza están formados principalmente por átomos de carbono. Muchos de ellos tienen su origen en plantas y animales, de ahí el nombre de compuestos orgánicos; por tanto, la química orgánica es una disciplina que estudia de forma detallada las sustancias constituidas por carbono.
Hay diferentes clases de compuestos orgánicos; estos se distinguen por un grupo de átomos que los conforma, ya que es el responsable de su comportamiento químico; dicho grupo se conoce como grupo funcional. Gran parte de los compuestos orgánicos está formado solo por átomos de carbono e hidrógeno y, por esta razón, se les denomina hidrocarburos (Chang, 2020).
Los hidrocarburos se dividen en dos tipos: alifáticos y aromáticos. Los primeros se estructuran a partir de cadenas lineales y no contienen anillo bencénico; además, se clasifican en alcanos, alquenos y alquinos. Los segundos, mientras tanto, son compuestos químicos con uno o más anillos bencénicos; algunos de los compuestos aromáticos más conocidos son los siguientes: benceno, fenol, tolueno y trinitrotolueno (TNT).
Tipos de enlace en los compuestos orgánicos
El enlace principal entre los hidrocarburos es el enlace covalente. En este, los átomos unidos comparten electrones para completar su último nivel, ya sea uno, dos o tres pares de electrones; de esta manera, generan enlaces sencillos, dobles o triples, respectivamente.
Funciones, estructura y nomenclatura de los compuestos orgánicos
Alcanos
Solo presentan enlaces covalentes sencillos y poseen la terminación -ano. Los alcanos tienen la fórmula general CnH2n+2, donde la n representa el número de carbonos de la molécula, es decir, para calcular la cantidad de hidrógenos se multiplica por dos el número de carbonos y, luego, se le suman dos más. Por ejemplo, el propano tiene tres carbonos, así que presenta ocho átomos de hidrógeno (Chang, 2020).
Nomenclatura IUPAC
Cabe mencionar que la nomenclatura de los compuestos orgánicos se basa en los lineamientos IUPAC (Unión Internacional de Química Pura y Aplicada). En el caso de los alcanos, los cuatro primeros compuestos no tienen nombres sistemáticos, es decir, el metano, etano, propano y butano, los cuales poseen uno, dos, tres y cuatro átomos de carbono, respectivamente (Chang, 2020).
Para el resto de los alcanos, se utilizan prefijos que señalan el número de átomos de carbono que los estructuran. Observa la tabla1:
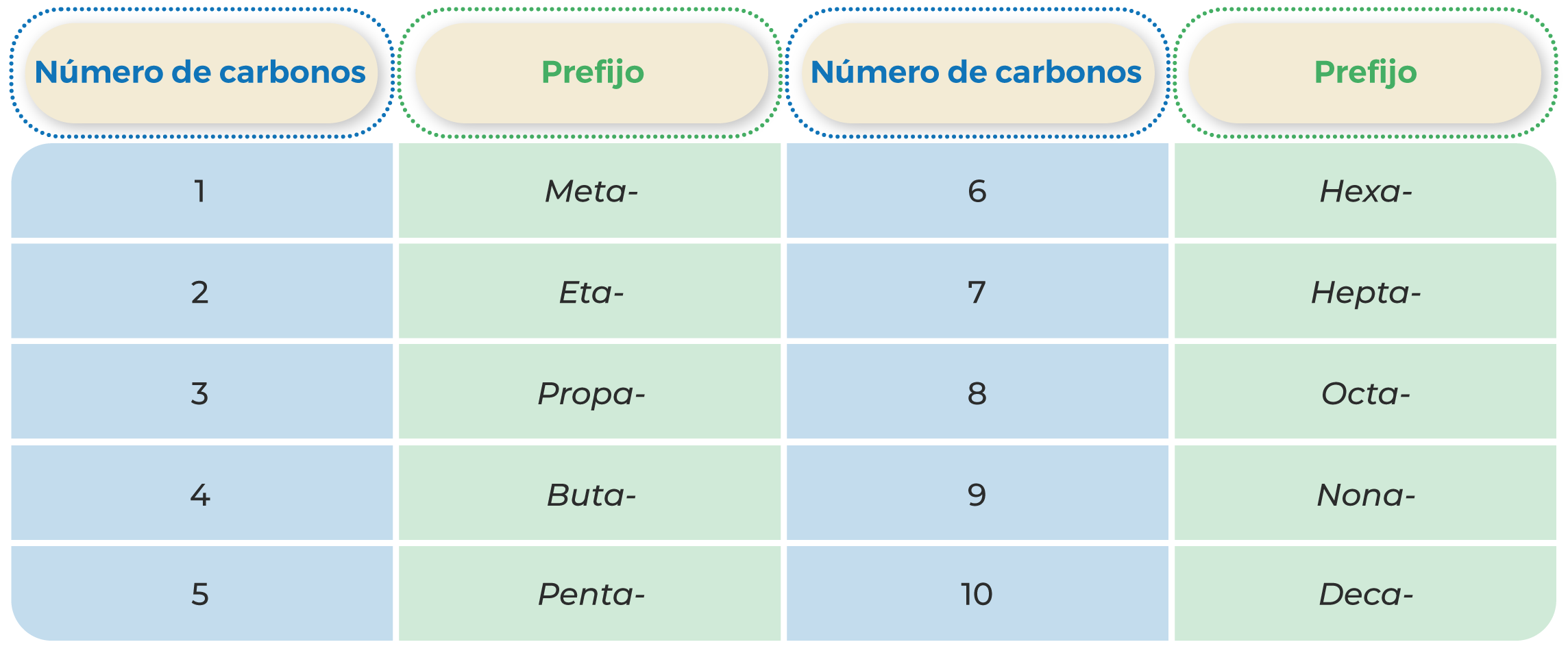
Tabla 1. Prefijos de hidrocarburos.
Fuente: Chang, R. (2020). Química (13ª ed.). Estados Unidos: McGraw-Hill.
Cuando los alcanos tienen ramificaciones, su nombre depende de cuántos átomos tiene la cadena más larga de carbono en la molécula.
Cuando un alcano pierde un átomo de hidrógeno, se le clasifica en el grupo alquilo, el cual puede unirse a una cadena más larga. Cuando en una cadena extensa sustituye a uno o más átomos de hidrógeno por otros grupos, el nombre del compuesto debe indicar la posición de los átomos de carbono donde ocurrió el reemplazo; después, se enumeran los átomos de carbono de la cadena más larga, partiendo del extremo donde las ramificaciones tengan los números más pequeños.
Si en los alcanos hay más de una ramificación de grupos alquilo del mismo tipo, se utilizan los prefijos di-, tri- o tetra- antes del nombre del grupo alquilo, ya que señalan las dos, tres o cuatro ramificaciones respectivas. Cuando hay dos o más grupos alquilo diferentes, sus nombres se colocan en orden alfabético; por ejemplo, el nombre de la molécula de 3 – etil- 2,3- dimetilpentano nos dice que la cadena más larga tiene 5 carbonos, que tiene un etil (en reemplazo de dos carbonos) en el 3 y tiene 2 metilos (en reemplazo de un carbono) en los carbonos 2 y 3.
Algunos alcanos no tienen extremos libres y sus átomos de carbono se unen formando anillos; a estos se les conoce como cicloalcanos. Para nombrarlos, se toma en cuenta el número de carbonos que forman el anillo y se les antepone el prefijo ciclo; por ejemplo, el ciclopentano es un compuesto formado por cinco carbonos dispuestos en un anillo.
Alquenos
Los hidrocarburos con, al menos, un enlace covalente doble carbono-carbono reciben el nombre de alquenos y su fórmula es CnH2n.
Los nombres de los alquenos poseen la terminación -eno y, para denominarlos, se señalan las posiciones de los enlaces dobles carbono-carbono. Para este grupo, el nombre se determina por el número de átomos de carbono en la cadena más larga, pues se indican aquellos donde están los enlaces dobles, considerando la dirección de la cadena cuyo número sea menor. Si presentan más de un enlace doble, se anotan las posiciones de los enlaces seguidos de los prefijos di-, tri- o tetra- (según tenga dos, tres o cuatro enlaces dobles) y la terminación -eno.
Alquinos
Los alquinos son hidrocarburos con, al menos, un enlace triple carbono-carbono y su fórmula general es CnH2n-2. Su nombre se determina a partir del número de átomos de carbono en la cadena más larga, pues indican la posición que ocupa el triple enlace carbono-carbono con el prefijo correspondiente a su número de carbonos y, por último, se añade la terminación -ino. Para anotar la posición de los átomos de carbono donde se localizan los enlaces triples, se considera la dirección de la cadena cuyos números sean los más pequeños. Al igual que en los alquenos, cuando se presentan más de un enlace triple, se escriben sus posiciones seguidas por los prefijos di-, tri- o tetra- (de acuerdo con el número de enlaces triples) y por la terminación correspondiente.
Compuestos aromáticos
Son un grupo grande de sustancias orgánicas, formadas a partir del benceno, es decir, de un compuesto cíclico estructurado por seis átomos de carbono. Para la nomenclatura de los bencenos, un átomo de hidrógeno se sustituye por otro átomo o grupo de átomos; entonces, se menciona el nombre del sustituyente, seguido del término benceno. Por ejemplo, metilbenceno.
Los carbonos en un anillo bencénico se nombran del uno al seis, asignándole el uno al carbono con un sustituyente y procurando que estos tengan los números más bajos. Si en un anillo bencénico hay dos sustituyentes, se utilizan los prefijos orto- (o), meta- (m) o para- (p), los cuales indican las posiciones relativas de ambos grupos. En este sentido, se utiliza el prefijo orto- cuando los sustituyentes se encuentran en los carbonos contiguos 1 y 2; meta-, cuando se encuentran en los carbonos 1 y 3; y para-, cuando tienen posiciones opuestas, es decir, en los carbonos 1 y 4.
Si el anillo bencénico se emplea como sustituyente, las sustancias generadas pertenecen al grupo fenilo; por su parte, a las sustancias donde los anillos bencénicos están fusionados se les llama policíclicos.
Alcoholes
Contienen el grupo funcional hidroxilo (-OH), les corresponde la terminación -ol y, entre sus miembros más conocidos, destaca el etanol o alcohol etílico. Los alcoholes funcionan como ácidos muy débiles, ya que no reaccionan con bases fuertes, como el hidróxido de sodio (NaOH), aunque sí lo hacen con los metales alcalinos, produciendo hidrógeno. Además, buena parte de estas sustancias resulta muy inflamable.
Para nombrar a los alcoholes, se sigue este procedimiento:
Éteres
Se forman por la unión de dos radicales mediante un átomo de oxígeno. Esto se representa con la fórmula R – O – R. Al igual que los alcoholes, los éteres son muy inflamables.
Para nombrar los éteres por la nomenclatura funcional, se mencionan los sustituyentes ordenados alfabéticamente y con la terminación éter; por ejemplo, el dietil éter proviene de la unión de dos etilos.
Aldehídos y cetonas
El grupo funcional de aldehídos y cetonas es el carbonilo, el cual consiste en un átomo de carbono, unido por un enlace doble a un átomo de oxígeno. En un aldehído, el oxígeno se enlaza con un carbono del extremo de la cadena; de esta manera, al menos un átomo de hidrógeno queda unido al carbono del grupo carbonilo.
Cuando se nombra a un aldehído, se escoge la cadena más larga que contenga este grupo y se le coloca la terminación -al o -dial, dependiendo de si tiene uno o dos.
Por otra parte, en las cetonas, el átomo de carbono del grupo carbonilo se une a los carbonos de dos grupos funcionales. Para nombrarlas, se selecciona la cadena más larga que contenga este grupo y se le añade la terminación -ona, -diona o -triona, según la cantidad de carbonilos que contenga; por ejemplo, propanona. También se pueden denominar mencionando los radicales que lo forman y agregando la terminación cetona; por ejemplo, dimetil cetona.
Ácidos carboxílicos
Los ácidos carboxílicos se pueden obtener por la oxidación de alcoholes o aldehídos y se caracterizan por contener el grupo funcional carboxilo (-COOH). Para nombrar los ácidos carboxílicos, se anota la cadena más larga que incluya a todos los grupos carboxilo y, después, se le agrega la terminación -oico o -dioico, según el número de carboxilos.
Ésteres
Están formados por la unión de dos hidrocarburos mediante un grupo COO, así que su fórmula general es R-COOR. Son muy utilizados en la manufactura de perfumes y agentes saborizantes, ya que el olor y sabor característicos de las frutas se deben a su presencia.
Para denominarlos, se nombra la parte del ácido con el sufijo -oato y la del alcohol con la terminación -ilo. Luego, se juntan ambas partes con la preposición de; por ejemplo, butanoato de etilo, la sustancia que da olor a la piña.
Aminas
Son compuestos con nitrógeno en su molécula y su fórmula general es R3N; en este caso, R puede ser H o un derivado de hidrocarburo. Estas sustancias se utilizan en la manufactura de colorantes; por ejemplo, de la anilina.
Las aminas con un solo grupo se nombran señalándolo con la terminación -amina; por ejemplo, etilamina. Si en la molécula hay dos o más grupos funcionales iguales, se usan los prefijos di- o tri-, según corresponda. Cuando tienen grupos diferentes, se ordenan alfabéticamente y se añade la terminación ya mencionada.
Amidas
Las amidas se obtienen al sustituir el grupo OH de un ácido carboxílico por uno NH3. La fórmula general de estos compuestos es RCONR’R’’; en este caso, las R representan radicales, el CO al grupo carbonilo y N al nitrógeno. Para denominarlas, se nombra el ácido carboxílico del que se derivan y se cambia la terminación -oico por la de -amida.
Macromoléculas
Los compuestos orgánicos forman las llamadas macromoléculas, las cuales son de gran tamaño y se estructuran a partir de numerosas partes pequeñas llamadas monómeros. Entre las macromoléculas, se encuentran tanto los plásticos como moléculas importantes para los seres vivos, como algunos polímeros de los carbohidratos (almidón y la celulosa), ácidos nucleicos y proteínas; los ácidos nucleicos son polímeros formados por monómeros llamados nucleótidos, mientras que las proteínas están estructuradas por unidades conocidas como aminoácidos.

Los compuestos orgánicos son sustancias muy frecuentes y utilizadas en la vida cotidiana. Al familiarizarte con sus nombres, podrás saber a qué grupo funcional pertenece cada sustancia y, al mismo tiempo, reconocer sus características; asimismo, te será más sencillo comprender la etiqueta de un producto alimenticio o una medicina, pues contienen varios de estos tipos de compuestos.

Asegúrate de:

