
 En la actualidad, los compuestos orgánicos utilizados en la vida cotidiana ofrecen una gran diversidad. Los alcoholes se emplean sobre todo en la industria farmacéutica, médica y cosmética; distintos sectores recurren a cetonas y aldehídos por sus aromas penetrantes, ya que además se encuentran con mucha facilidad en el medio ambiente; los ácidos son sustancias frecuentes en las industrias alimenticia y química, pues producen las reacciones necesarias para generar ciertas sustancias y materiales. Debido a sus múltiples aplicaciones, se necesita identificarlos estructuralmente y nombrarlos, así que a lo largo de este tema comprenderás cómo hacerlo.
En la actualidad, los compuestos orgánicos utilizados en la vida cotidiana ofrecen una gran diversidad. Los alcoholes se emplean sobre todo en la industria farmacéutica, médica y cosmética; distintos sectores recurren a cetonas y aldehídos por sus aromas penetrantes, ya que además se encuentran con mucha facilidad en el medio ambiente; los ácidos son sustancias frecuentes en las industrias alimenticia y química, pues producen las reacciones necesarias para generar ciertas sustancias y materiales. Debido a sus múltiples aplicaciones, se necesita identificarlos estructuralmente y nombrarlos, así que a lo largo de este tema comprenderás cómo hacerlo.

Estructura y descripción de grupos funcionales
 Los grupos funcionales se definen como uniones de átomos que muestran propiedades y reactividad química consistente. Las grandes moléculas presentes en la naturaleza y las generadas de manera artificial pueden contener diferentes tipos de grupos funcionales; al estudiar su acomodo y combinación se han producido millones de compuestos con características únicas de solubilidad, reactividad, estabilidad y, sobre todo, de actividad biológica variada. Las investigaciones en torno a los diferentes grupos funcionales han ayudado a los científicos a fabricar nuevas sustancias, como los antibióticos, que han logrado salvar millones de vidas; por ello, conocer su estructura y nomenclatura es muy valioso para todos (Chang, 2020).
Los grupos funcionales se definen como uniones de átomos que muestran propiedades y reactividad química consistente. Las grandes moléculas presentes en la naturaleza y las generadas de manera artificial pueden contener diferentes tipos de grupos funcionales; al estudiar su acomodo y combinación se han producido millones de compuestos con características únicas de solubilidad, reactividad, estabilidad y, sobre todo, de actividad biológica variada. Las investigaciones en torno a los diferentes grupos funcionales han ayudado a los científicos a fabricar nuevas sustancias, como los antibióticos, que han logrado salvar millones de vidas; por ello, conocer su estructura y nomenclatura es muy valioso para todos (Chang, 2020).
Grupos funcionales del carbono
Este concepto se refiere a los enlaces dobles o triples entre los átomos y sus combinaciones, ya que siempre reaccionarán de una forma determinada; además, esta parte de la estructura se encarga de proporcionar nombre, propiedades y características a la molécula. Los compuestos orgánicos se clasifican según el grupo funcional que posean en su estructura; sin embargo, muchos cuentan con más de uno. A continuación, se resumen de manera muy concreta los diferentes grupos funcionales.
Alcohol
En su estructura de hidrocarburo, estas sustancias poseen un grupo funcional denominado hidroxilo (-OH). En este sentido, se clasifican dependiendo de la posición que ocupa este grupo: son primarios si se une a un carbono primario (carbono con tres hidrógenos); secundario, si lo hace a un carbono secundario (carbono con dos hidrógenos); o terciario, si se asocia con un carbono terciario (carbono sin hidrógenos). Otra forma de organizarlos es a partir de los grupos hidroxilos presentes en la estructura. De esta manera, si cuentan con más de un grupo -OH se les denomina polioles; con dos, glicoles; con tres, trioles; con cuatro, tetraoles; y así sucesivamente.
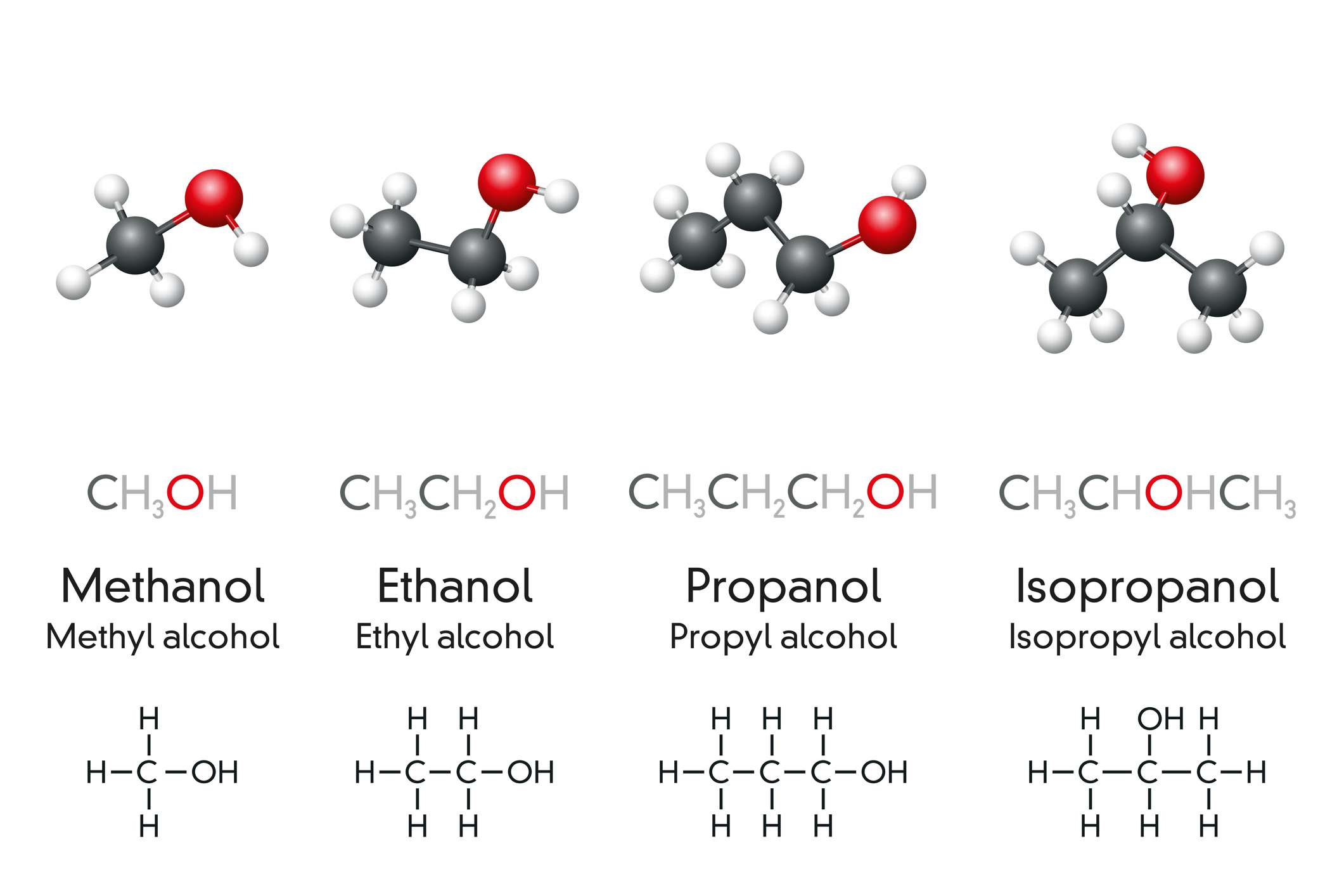
Imagen 1. Primeros cuatro alcoholes: metanol (alcohol primario), etanol y propanol (alcoholes secundarios), así como isopropanol (alcohol terciario).
Los usos de estas sustancias son muy variados; por ejemplo, la industria farmacéutica emplea el alcohol etílico para desinfectar heridas y superficies, mientras que la automotriz recurre al etilenglicol para fabricar anticongelantes.
Nomenclatura IUPAC
La Unión Internacional de Química Pura Aplicada (IUPAC) establece una serie de pasos para nombrar a los alcoholes:
Éteres
En su estructura de hidrocarburo, los éteres cuentan con el grupo funcional (R-O-R), donde R representa un hidrocarburo y O al oxígeno; cabe mencionar que las cadenas R pueden ser iguales o distintas (éteres simples o simétricos). Estos compuestos se utilizan en la industria química como solventes para separar mezclas orgánicas; entre ellos, destacan el eugenol, presente en la esencia del clavo tan común en la cocina mexicana, y el tetrahidrocannabinol, principio activo de la marihuana.
Nomenclatura IUPAC
Ejemplo:
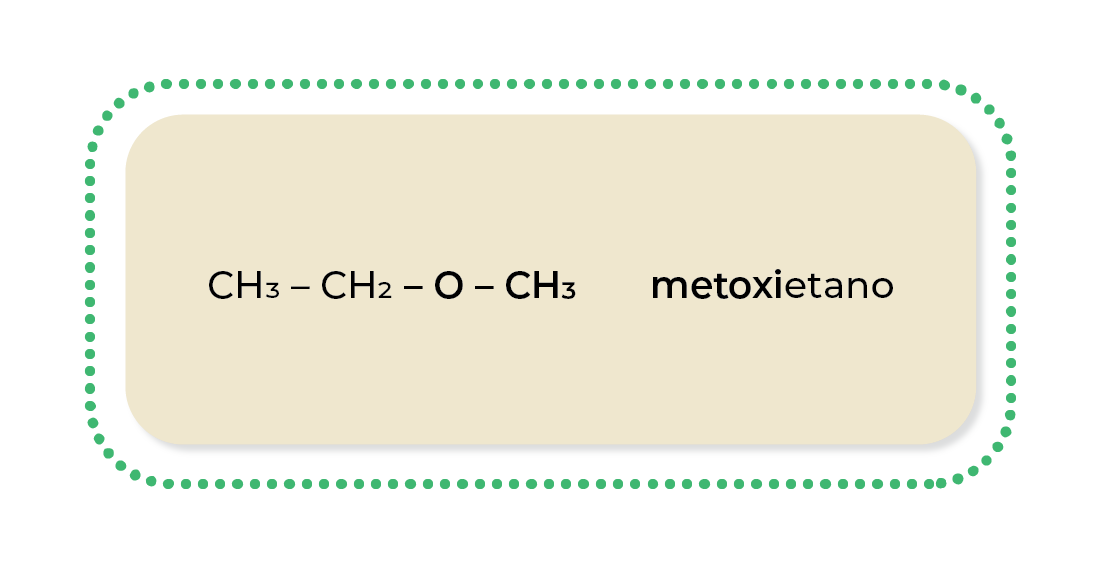
Aldehídos
En su estructura de hidrocarburo, los aldehídos poseen el grupo funcional denominado formilo (R-CHO), con un doble enlace entre el carbono y el oxígeno C=O. Se trata de compuestos polares, así que se disuelven bien en agua y esta característica les ha valido una gran amplitud de usos; por ejemplo, el metanal o formaldehído sirve para preservar cadáveres y alimentos, aunque también se emplea en la industria textil y se encuentra presente en la vainilla (como saborizante).
Nomenclatura IUPAC
En este grupo funcional de la cadena principal, el carbono unido al oxígeno siempre aparece al final; por tanto, no se necesita especificar su ubicación. Para nombrarlo, primero se selecciona la cadena más larga con el grupo aldehído, se elige el nombre que corresponda al tipo de hidrocarburo (alcano, alqueno o alquino) y se cambia la terminación por -al o -dial (si son dos).
Ejemplo:
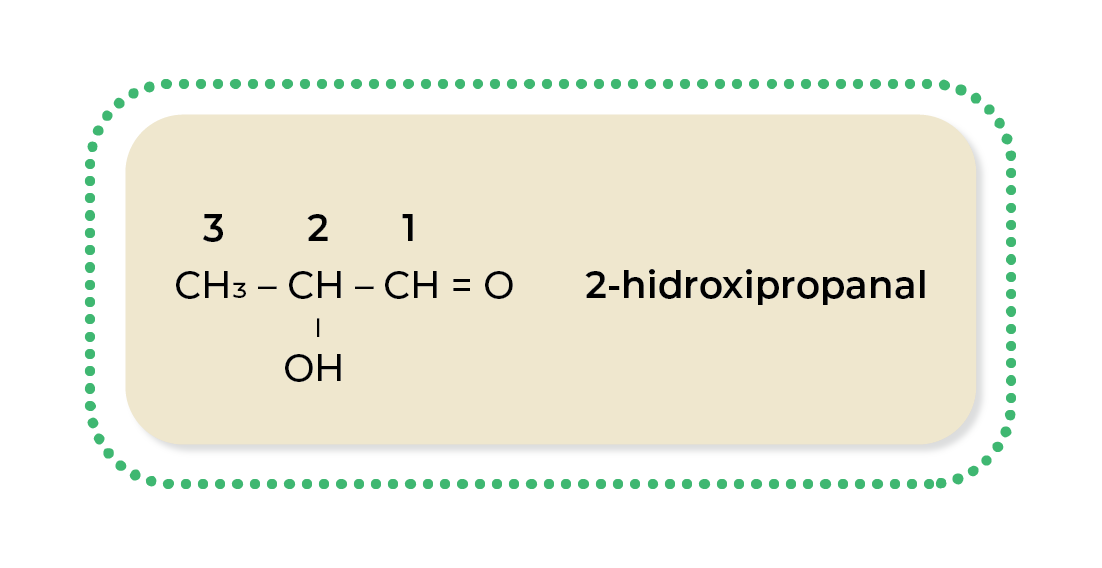
Cetonas
Al igual que los aldehídos, las cetonas presentan el grupo carbonilo C=O, aunque su fórmula es R-CO-R. En este caso, se distingue del grupo anterior porque el átomo de oxígeno se une a un carbono intermedio y no al terminal. Entre las cetonas más conocidas, se encuentran la fructosa, que proporciona dulzor a las frutas, y hormonas como la progesterona y testosterona, que originan las características sexuales en mujeres y hombres.
Nomenclatura IUPAC
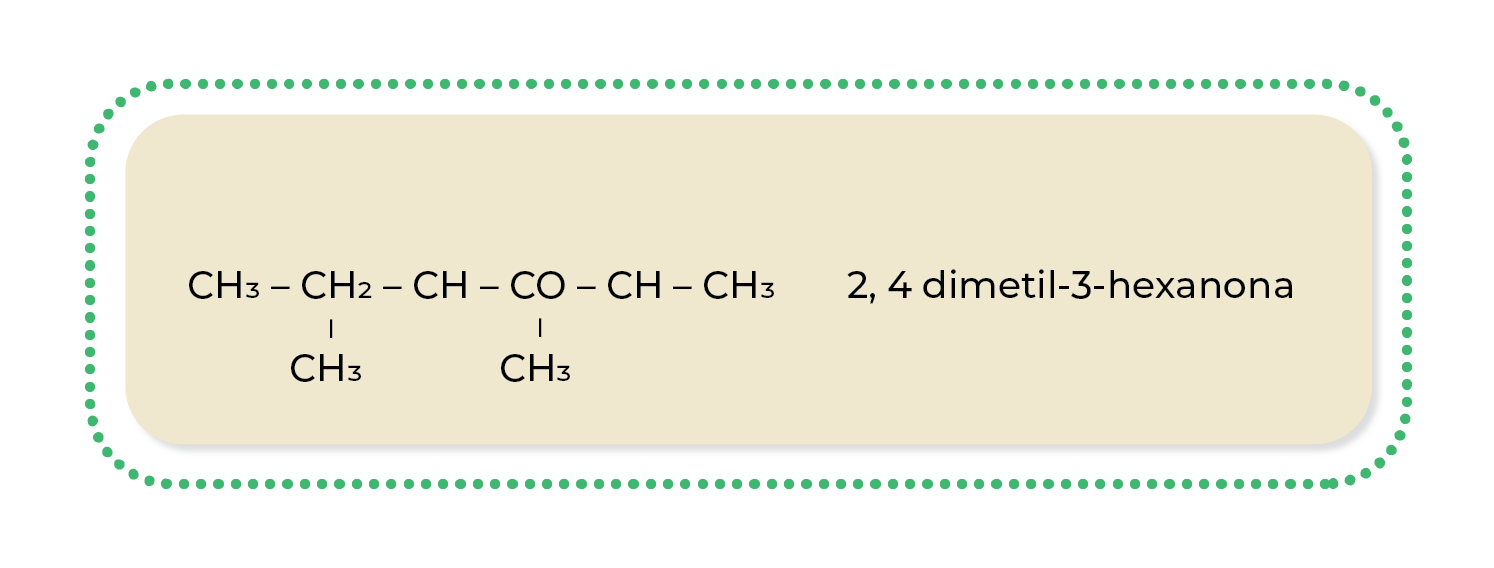
Para nombrar a estos compuestos, primero se selecciona la cadena más larga que contenga al grupo (o grupos) carbonilo y se considerará la cadena principal. Como en los casos anteriores, el nombra se elige según el tipo de hidrocarburo al que pertenezca (alcano, alqueno o alquino) y solo se cambia su terminación a partir del número de grupos carbonilos presentes en la estructura (-ona, -diona, -triona, -tetraona, etcétera).
Ejemplo:
Ácidos carboxílicos
Los compuestos pertenecientes a este grupo funcional poseen en su estructura el grupo carboxilo (-COOH). Son fundamentales en la industria, ya que generan una amplia gama de grupos funcionales distintos, como ésteres y aminas, muy importantes en la industria médica. Los ácidos carboxílicos se generan a partir de la oxidación del grupo aldehído; entre los más sobresalientes, figura el ácido metanoico, que se emplea en la industria textil, mientras que en la naturaleza se halla en las hormigas, pues es el responsable del ardor cuando estos insectos pican.
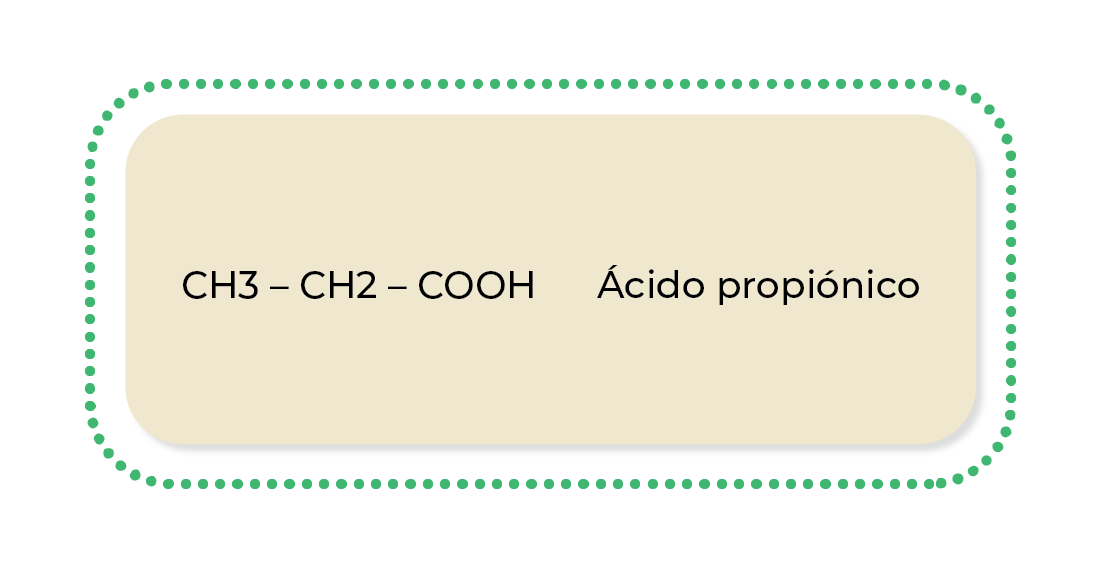
Nomenclatura IUPAC:
Ejemplo:
Ésteres
Los ésteres se forman por la unión de un ácido carboxílico con un alcohol y, de hecho, se consideran derivados de los ácidos; su fórmula es R-CO-O-R. Es muy importante reconocer las partes correspondientes al ácido y al alcohol, ya que se necesitan para otorgar un nombre al compuesto. Una forma de identificarlos es a partir del carbono que se une con los oxígenos: la parte con doble enlace pertenece al ácido y la del enlace simple corresponde al alcohol. Los ésteres se utilizan en varios productos, desde solventes hasta aromatizantes frutales en artículos de higiene personal, como perfumes, jabones y cremas.
Nomenclatura IUPAC
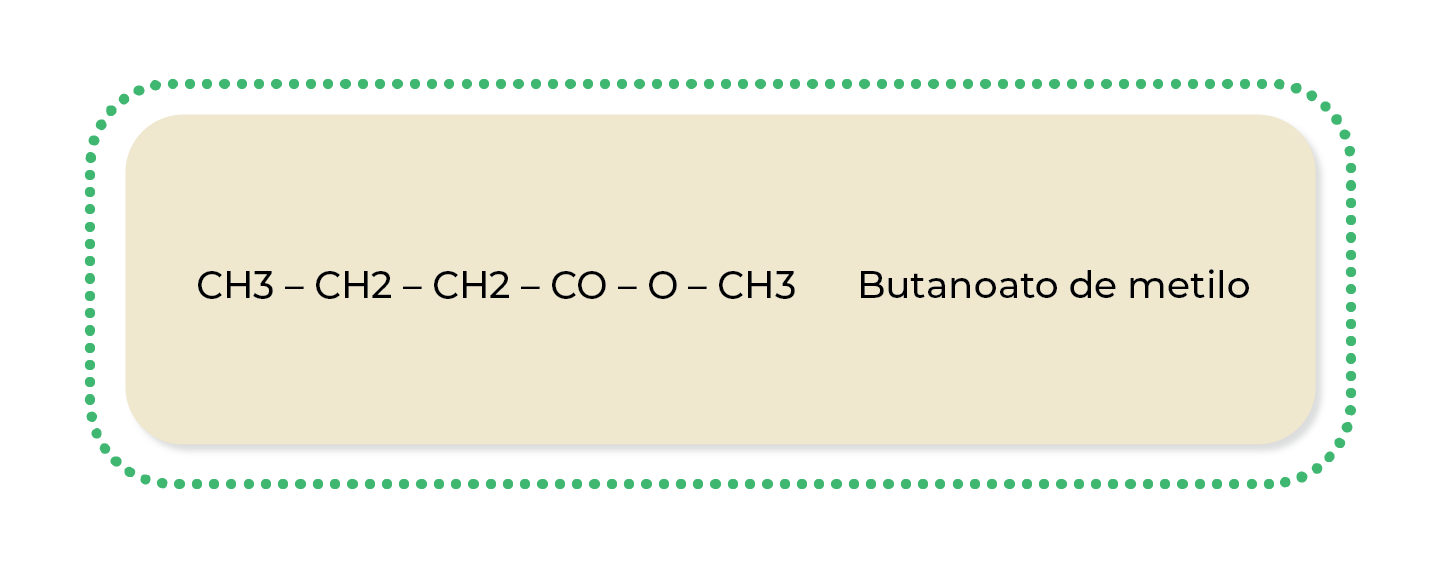
Primero se escribe la parte que corresponde al ácido y, después, la del alcohol; cabe mencionar que la enumeración debe iniciar por el grupo éster. A la sección del ácido se le da la terminación -oato, mientras que a la del alcohol la de -ilo. Finalmente, el nombre se dispone como si el ácido formara parte del alcohol.
Ejemplo:
Aminas
Estas sustancias contienen nitrógeno (N) en su estructura y se derivan del amoniaco (NH3). Se clasifican en primarias, si se encuentran unidas a una cadena de hidrocarburo y pierden un hidrógeno; secundarias, si se unen a dos cadenas carbonadas con un solo hidrógeno; y terciarias, si se asocian a tres cadenas carbonadas cuando el nitrógeno pierde sus tres hidrógenos. Las aminas se utilizan en productos antigripales, como la histamina. Nomenclatura IUPAC:
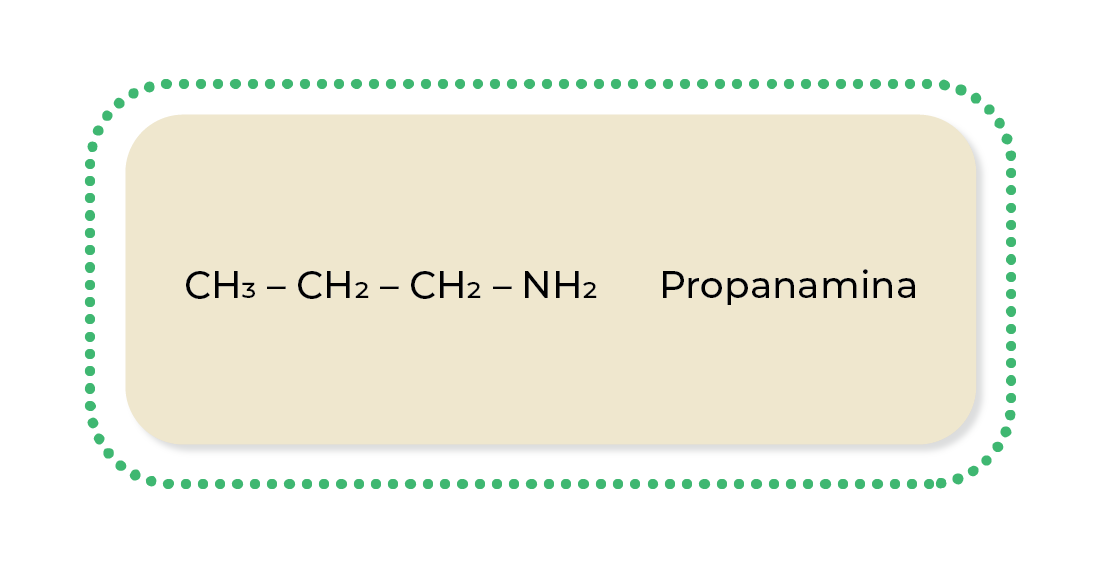
Aminas primarias: se nombra al radical a partir de su hidrocarburo correspondiente (alcano, alqueno o alquino) y se cambia su terminación por -amina.
Ejemplo:
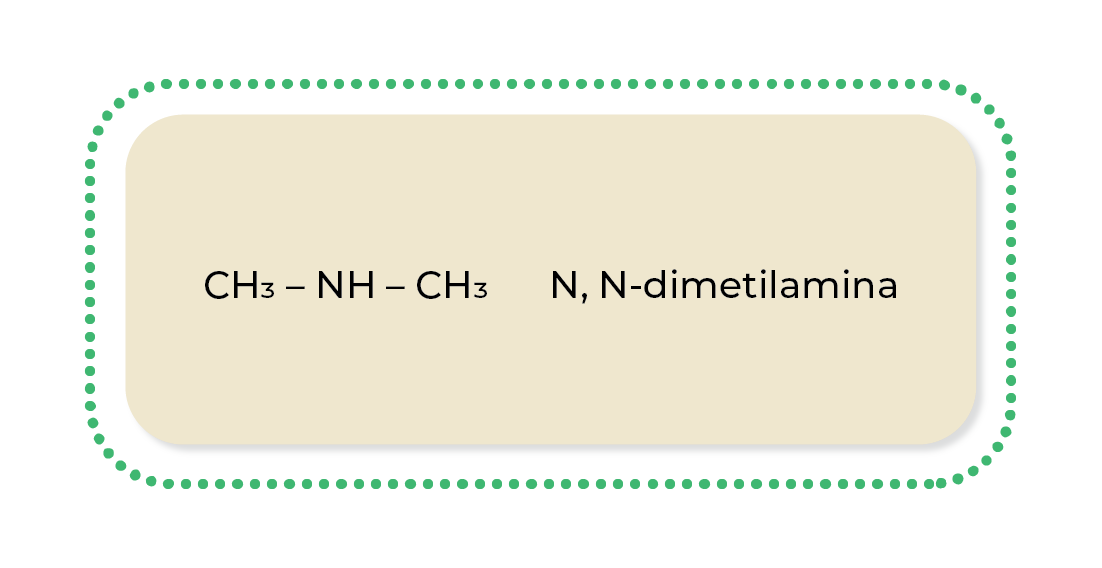
Aminas secundarias: se utiliza el prefijo N, que indica que las cadenas carbonadas están unidas al nitrógeno.
Ejemplo:
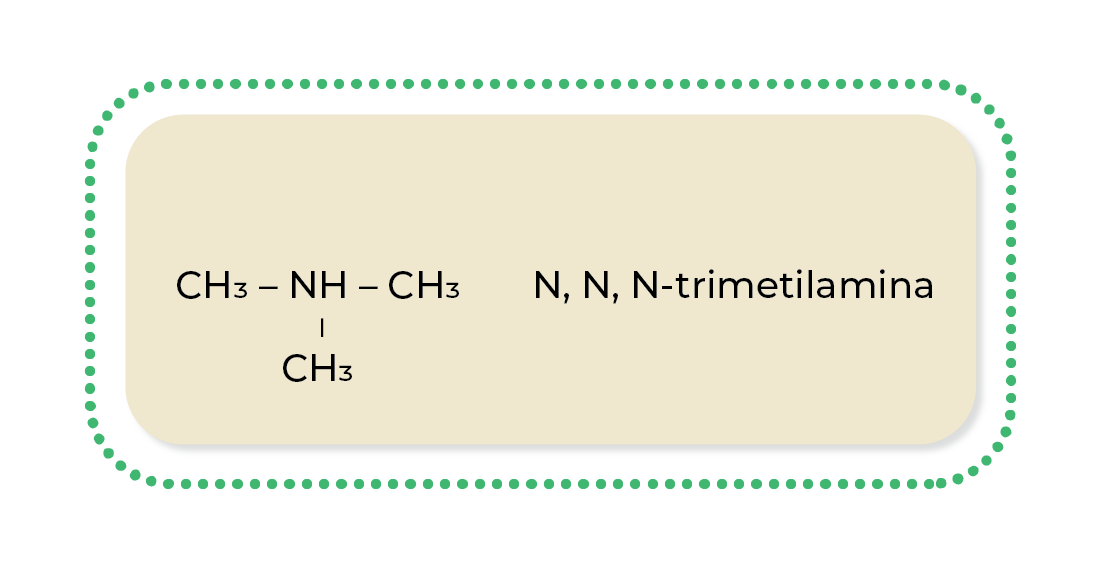
Aminas terciarias: se utiliza el prefijo N, N, N; esto indica que las cadenas carbonadas están unidas al nitrógeno.
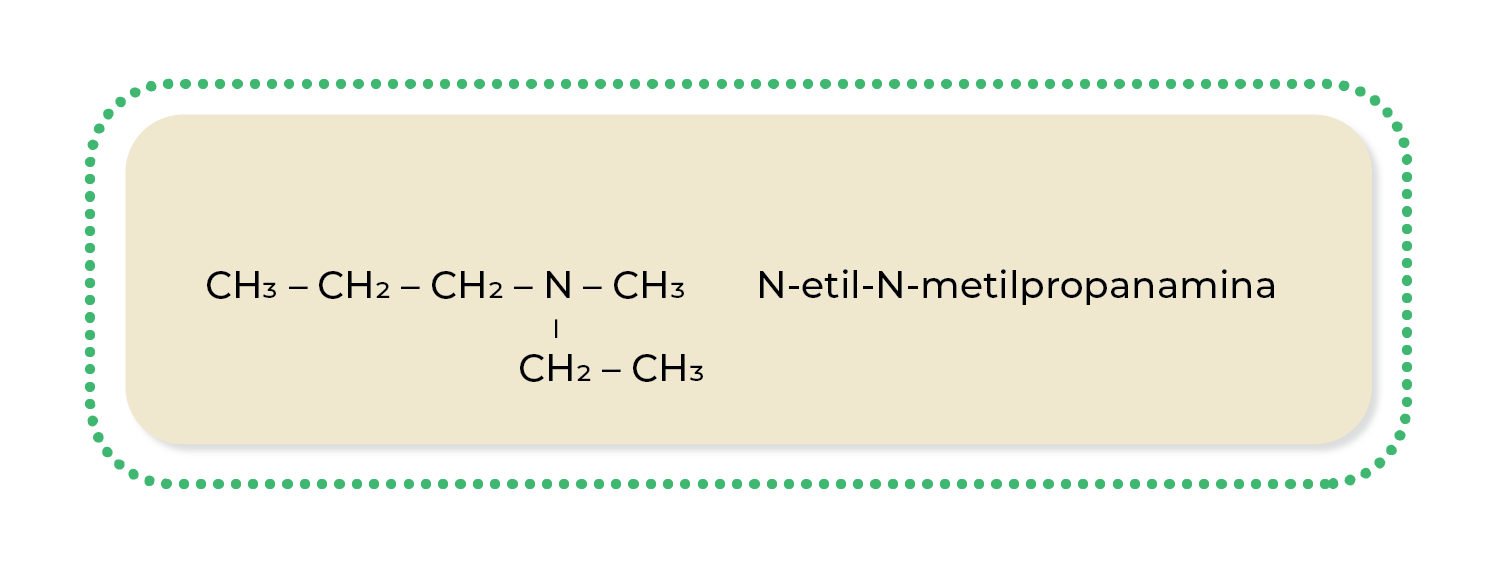
Cuando una de las cadenas carbonadas es distinta, se elige como principal a la más larga y las otras se nombran por orden alfabético, utilizando el símbolo N y la terminación -amina.
Ejemplo:
Amidas
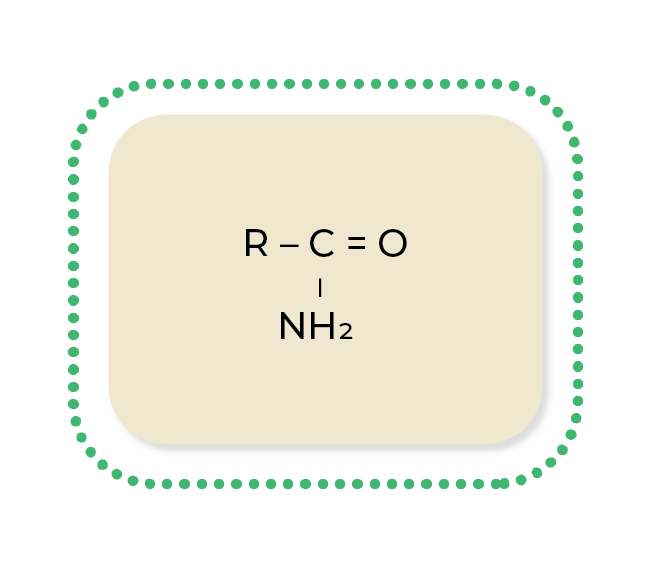
Estos compuestos se originan al sustituir el grupo hidroxilo (-OH) de un ácido carboxílico por el grupo -NH2 de una amina. Las amidas tienen varios usos, desde explosivos como la etanamida, hasta antibióticos como la penicilina y la cefalosporina. Su fórmula general es esta:
Nomenclatura IUPAC
Primero, la cadena con el grupo amida se selecciona como principal y, después, se siguen los mismos pasos que en los ácidos carboxílicos; sin embargo, se elimina la palabra ácido y se reemplaza la terminación -oico por la de -amida. En las amidas secundarias, las cadenas carbonadas se ordenan de manera alfabética, anteponiendo el símbolo N. La cadena más grande y con el grupo amida se considera la principal.
Ejemplo:
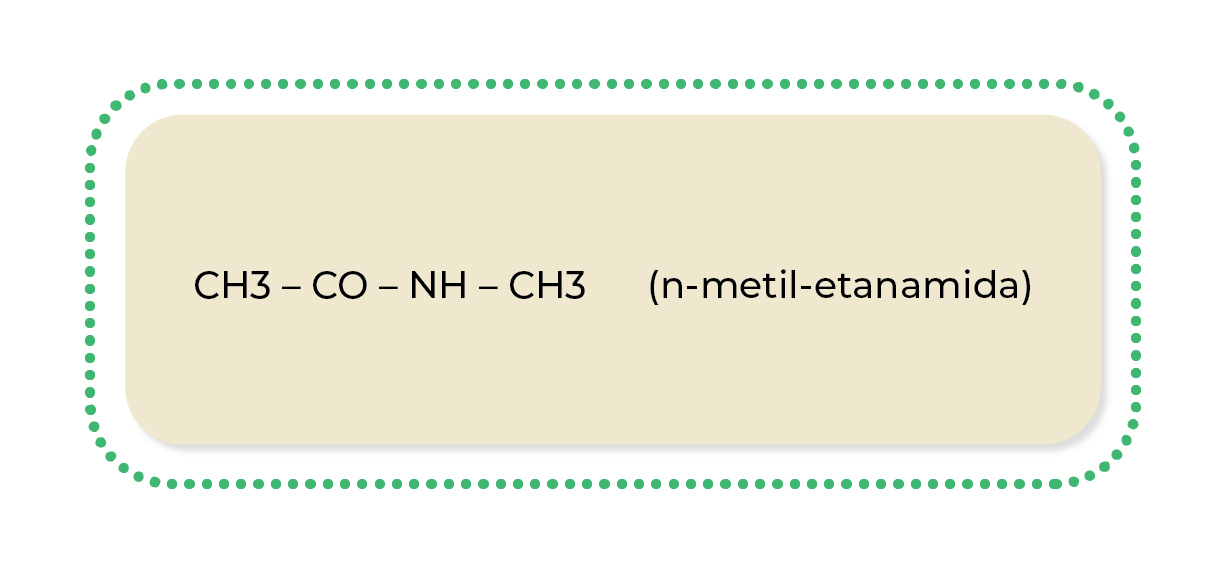
La siguiente tabla resume todo lo expuesto en este tema:
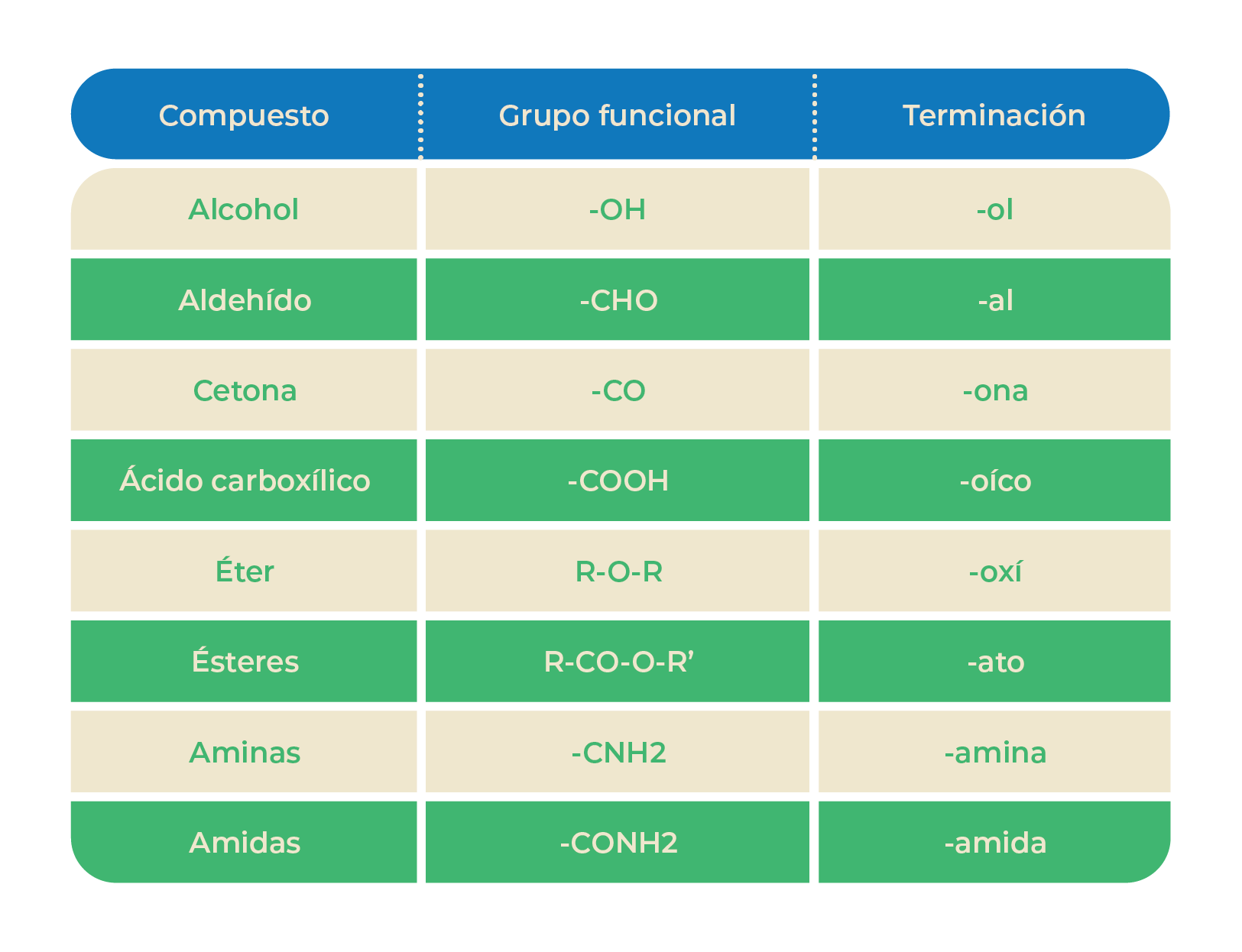
Tabla1. Grupos funcionales.

Como te habrás dado cuenta, el estudio de los diferentes grupos funcionales resulta esencial para la industria, ya que se emplean en varios sectores, desde el farmacéutico (antigripales) hasta el de la industria textil (solventes y colorantes). De igual forma, su distribución en la naturaleza es diversa, pues se encuentran presentes tanto en los sabores frutales como en la picadura de una hormiga. El estudio de estos compuestos hace más sencilla la vida, ya que muchos medicamentos naturales pertenecen a dichos grupos. La ciencia los ha descubierto y modificado para mejorar su eficacia, lo cual salva a muchas personas diariamente, como ocurre con los antibióticos.

Asegúrate de:

